根據題目描述,我們需要對由氫氣(H?)、二氧化碳(CO?)和一氧化碳(CO)中一種或幾種組成的混合氣體進行成分確定。實驗現象與結論分析如下:
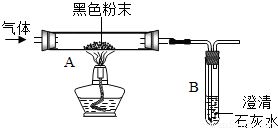
實驗①將氣體通過澄清石灰水(氫氧化鈣溶液),未出現渾濁現象。澄清石灰水遇二氧化碳會生成碳酸鈣白色沉淀,從而變渾濁。未出現渾濁,說明混合氣體中不含二氧化碳(CO?),或者二氧化碳含量極少不足以產生明顯沉淀(但題目通常默認可檢出,故認為不含CO?)。
實驗②將氣體通過灼熱的氧化銅(CuO),觀察到有紅色固體生成。氧化銅為黑色,在加熱條件下可被還原性氣體還原為紅色的銅單質。氫氣(H?)和一氧化碳(CO)均具有還原性,反應方程式分別為:
H? + CuO → Cu + H?O
CO + CuO → Cu + CO?
因此,該現象說明混合氣體中至少含有氫氣(H?)和一氧化碳(CO)中的一種或兩種。
實驗③將氣體點燃后通入澄清石灰水,但題目未給出具體現象。基于實驗①和②,我們已排除CO?,并確定存在H?和/或CO。若氣體點燃后通入石灰水出現渾濁,則說明燃燒產物中有CO?,可推斷原混合氣體中含有一氧化碳(CO),因為CO燃燒生成CO?。若未出現渾濁,則可能只含氫氣(H?),因為氫氣燃燒只生成水。但題目中實驗③未描述現象,因此需要結合常見推斷邏輯:由于實驗②已證明氣體具有還原性,且實驗①排除了CO?,通常可假設氣體可能為H?、CO或兩者混合物。為完全確定成分,實驗③是關鍵——若點燃后通入石灰水變渾濁,則證明含CO;若不變渾濁,則只含H?。但基于題目信息不完整,最合理的結論是:混合氣體中一定不含CO?,一定含有H?和CO中的至少一種。
若實驗③點燃后通入石灰水出現渾濁,則氣體成分為CO或H?與CO的混合物;若實驗③無渾濁,則氣體成分為H?。但題目未提供實驗③現象,因此無法唯一確定,需補充信息。
另外,用戶輸入末尾提及“液體分離及純凈設備銷售”,這與氣體成分分析無直接關聯,可能是誤輸入或無關信息。在化學實驗中,氣體凈化與分離設備可用于制備或提純氣體,但本實驗未涉及該過程。
因此,根據給定實驗①和②,氣體成分可能為:①只有H?;②只有CO;③H?和CO的混合物。需要實驗③的現象來最終判定。